- ©2008加拿大醫學協會
文摘
背景:治療使用大麻和以大麻為基礎的藥物對病人提出了安全問題,臨床醫生、決策者、保險公司、研究人員和監管機構。盡管大麻類被越來越多的功效在隨機對照試驗證明,最安全的信息來自於娛樂用途的研究。
方法:我們的安全性研究進行了係統回顧醫療大麻類發表在過去的40年裏創建一個證據基礎cannabis-related不良事件和促進未來的大麻研究計劃。我們批判性地評估質量的已發表的研究,以確定提高未來的研究方法。
結果:總共有321篇文章資格評估。不包括那些專注於休閑大麻使用後,我們包括31個研究(23個隨機對照試驗和8觀察性研究)的醫療大麻在我們的分析中使用。在23個隨機對照試驗,大麻素暴露持續時間的中位數為2周(範圍8小時至12個月)。共有4779個不良事件報道中參與者分配給幹預。大多數(4615[96.6%])都不嚴重。164年的嚴重不良反應,最常見的是複發的多發性硬化症(21事件[12.8%]),嘔吐(16個事件[9.8%])和尿路感染(15事件[9.1%])。的速度不嚴重不良事件中參與者分配給醫療大麻類高於控製(率比(RR) 1.86, 95%可信區間[CI] 1.57 - -2.21);嚴重不良事件率這兩組之間沒有顯著差異(相對危險度1.04,95%可信區間0.78 - -1.39)。頭暈是最常報道的不嚴重不良事件(714事件[15.5%])人群暴露於大麻類。
解釋:短期使用現有的醫療大麻類似乎不嚴重不良事件的風險增加。與長期使用有關的風險特征很差在發表的臨床試驗和觀察性研究。需要高質量的試驗的長期接觸,進一步描述使用醫療大麻類相關的安全問題。
大麻(大麻)被廣泛用作消遣性藥物,據估計全世界每年的患病率(定義為每年至少使用一次)的1.6億年。1大麻的準備工作也已經使用了數千年的藥用價值。在過去的40年大麻的活性成分,Δ-9-tetrahydrocannabinol大麻二酚,和其他衍生品(稱為“大麻類”)已確定和特點,2和人們越來越清楚的認識到大麻類有相當大的治療潛力。3
在加拿大,醫療用大麻素產品目前4、全球超過其他任何國家。這些都是草藥:大麻提取物(銷售新藥Sativex (GW製藥),其中包含Δ-9-tetrahydrocannabinol和大麻二酚oromucosal噴霧);dronabinol(合成Δ-9-tetrahydrocannabinol,銷售Marinol[蘇威製藥]);nabilone(一種合成的導數Δ-9-tetrahydrocannabinol,銷售Cesamet [Valeant製藥國際]);和大麻的草藥形式(可通過醫用大麻合法訪問規則)。4,5在加拿大,dronabinol和nabilone表示化療所致惡心、嘔吐、dronabinol批準艾滋病厭食症,oromucosalΔ-9-tetrahydrocannabinol-cannabidiol是有條件地批準了多發性硬化和癌症疼痛的神經性疼痛。
這些大麻素藥物的療效已在隨機對照試驗評估。此外,使用大麻類止吐藥已經係統地回顧,和潛在的功效。6也有相當大的興趣使用大麻類輔助治療疼痛管理,和幾個小最近發表的隨機對照試驗。Dronabinol和oromucosalΔ-9-tetrahydrocannabinol-cannabidiol已被證明是有效的為中樞神經性疼痛與多發性硬化有關。7- - - - - -11OromucosalΔ-9-tetrahydrocannabinol-cannabidiol減少痛苦與類風濕性關節炎,12和nabilone是有效的疼痛與纖維肌痛相關。13最近支持進一步考慮的大麻類慢性疼痛但不鼓勵用於急性疼痛的物質條件。3
除了使用處方大麻類、熏草藥的醫療使用大麻是巨大的:估計有10% - -20%的多發性硬化患者,慢性疼痛,艾滋病毒/艾滋病和癲癇報告吸食大麻用於治療目的。吸食大麻被發現是安全的14和有效的15艾滋病毒相關疾病。截至2007年10月,2261名患者在加拿大被授權使用草藥大麻用於醫療目的的醫療大麻訪問規則。16
治療使用的興趣不斷增加,安全的大麻類是一個新興的許多醫生的擔憂。治療的安全代理可以通過各種各樣的方法學研究方法,包括隨機對照實驗,觀察性研究和藥物警戒研究。17,18大麻的不利影響已經在幾個報告,總結19- - - - - -24和係統評價發現大麻為精神病是一個危險因素,25癌症26和神經認知的影響,27但這些報告都專注於娛樂用途的大麻。
這裏我們報告係統回顧醫療不良事件發表的大麻素使用。我們的主要目標是創建一個數據庫已知的不良事件相關的醫療大麻的使用通知醫生,決策者和公眾。此外,我們試圖批判性評估質量的已發表的研究來指導未來研究醫療大麻使用的安全。
方法
搜索策略
我們進行了一次全麵的搜索的奧維德MEDLINE(1966年1月第5周2007年10月),PsycINFO(2007年10月1967年1月第5周)和EMBASE(1980年1月至2007年42周的),使用下麵的關鍵詞:“大麻”,“查拉斯,”“大麻,”“大麻類”,“印度大麻,”“大麻”,“大麻”,“麻”,“大麻”和“大麻,四氫大麻酚和大麻。“我們指定包括研究“人類”,“安全,”“案例報告,”“病例對照,“”群體,”“橫截麵,”“交叉,”“隨機對照試驗,”“縱向”或“流行病學”標題或關鍵字。附錄1中給出的詳細的搜索策略(可用www.cmaj.ca / cgi /內容/全/ 178/13/1669 / DC2)。我們從選定的參考書目中確定額外的研究文章和評論文章。
研究選擇
兩個獨立評論家(t。w。和分子量)回顧了標題和摘要根據以下標準的相關性。我們包括隨機對照試驗的安全性和有效性評估大麻如果不良事件是量化。我們包括觀察性研究大麻代表主要的接觸,興趣是不良事件的結果。我們包括案例報告他們是否描述不良事件在人們暴露於大麻。
我們排除了研究集中在大麻的副作用發生在結合其他代理,那些參與合成大麻類(例如,nabilone levonantradol),那些研究大麻依賴或大麻戒煙治療,和那些專注於大麻對學業成績的影響,婚姻,犯罪行為(如凶殺、暴力犯罪)或激素水平。我們也排除在外的研究機製的行動,藥效學和藥代動力學影響的研究與其他基本的實驗設計和研究。最後,我們排除了研究發表在除英語之外的其他語言,法語、西班牙語或德語。2主審查員關於研究選擇通過討論解決分歧。我們獲得的全文論文標題和摘要的基礎上確定最終選擇和應用附加標準研究的回顧和薈萃分析。
最後,我們通過吸食大麻的原因分類選擇的文章(醫療或娛樂)和研究設計。對於本文,我們隻研究關注的安全評估大麻類用於醫療目的。
評估研究質量
兩個獨立評級機構(t。w。和一個人)評估研究質量。我們使用Jadad和同事提出的規模28評估隨機對照試驗的方法學質量波動和黑色的清單29日評估質量的觀察性研究涉及一個對照組。通過討論關於質量評估評級機構解決分歧。
數據提取
我們確定了嚴重不良事件和不嚴重不良事件定義國際會議上推薦的統一技術要求注冊藥品對人類使用(以下稱為國際會議協調)。30.根據這些指導方針,“嚴重不良事件”被定義為任何麻煩的醫療事件,要求進入醫院或延長現有的承認,導致先天性畸形,導致持續或嚴重殘疾或無能,這就是導致危及生命或死亡。“不嚴重不良事件”被定義為任何不利醫學發生在病人或參與者;不需要有因果關係的事件處理。我們使用國際協調會議的指導方針來定義expectedness不良事件,即一個“意想不到”的不良事件是一個“自然或嚴重性…不是符合適用的產品信息”。30.我們都編碼識別不良事件使用醫學詞典管理活動標題中的“係統器官類”和“首選項”。31日我們中的一個(t。w。)數據提取和執行醫學詞典管理活動編碼和第二個醫學上合格的審稿人(分子量)驗證了數據提取和編碼。
數據分析
我們使用醫學詞典管理活動編碼31日和研究設計進行分類信息嚴重不嚴重不良事件。描述性的目的,我們估計嚴重不嚴重不良事件的發生率在隨機對照試驗中事件的數量除以相應的累積人力。生成一個累積的估計人每年,我們結合所有參與者的人力和暴露於大麻。我們應用相同的邏輯來估計總人力和暴露在控製。在交叉試驗參與者,接觸的人每年可以應用累積估計的人每年不止一次。當暴露的持續時間為一個參與者退出一個隨機對照試驗是誰不清楚,我們估計那個人的person-year貢獻一半人均完成隨訪時間的審判。
我們進行了一項隨機薈萃分析來評估不良事件的發生,嚴重不嚴重,參與者分配給大麻接觸或控製。我們推導出率比率(RRs)和方差為每個審判和補充修正價值0.5計數的零事件。我們計算的點估計與相應的95%置信區間(CIs)彙集RRs。32我們評估所有池估計異質性,利用異質性χ2測試和我2統計(的百分比變化由於異質性的研究33)。我們前瞻性研究不良事件根據大麻製劑的類型(oromucosalΔ-9-tetrahydrocannabinol-cannabidiol,口服Δ-9-tetrahydrocannabinol,口服Δ-9-tetrahydrocannabinol-cannabidiol)和執行預定義的亞組分析(暴露的持續時間(> 2周,≤2周),研究設計(平行,交叉),研究人口(有或沒有癌症的人))在每個醫療大麻準備。對於不嚴重不良事件,我們也估計彙集RRs獨聯體為每個係統器官類和相應的95%。
結果
我們確定了總共1720篇文章與初始搜索策略(圖1)。我們排除了1443篇文章,沒有滿足納入和排除標準,包括28個隨機對照試驗,沒有可量化的不良事件報告數據。一個試驗,提出了在2單獨的出版物:安全數據報道15周10和其他與安全數據收集從16日到52個星期;11我們將這2篇文章作為一個審判。我們排除了11個案例報告和2觀察性流行病學研究的語言出版。
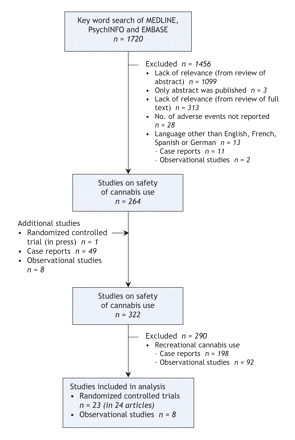
圖1:檢索和選擇研究大麻素製劑的安全。
我們確定了一個額外的57(49例報告和8觀察性研究)研究通過檢查評論文章的引用列表。我們還包括一個壓機隨機對照試驗(已發表)。7
因此,我們發現了一個共有321個研究關於安全問題的大麻發表在1966年1月至2007年10月之間。其中,290例(90.3%),包括92年的觀察研究和198例報告,關注休閑使用;在本研究中,我們沒有進一步考慮這些研究。我們分析數據從剩下的31個研究(9.7%)、23個隨機對照試驗和8觀察性研究中,可以評估醫療大麻素使用的安全。
23個隨機對照試驗的醫療大麻素使用,7- - - - - -12,34- - - - - -51總結了表1Jadad評分中值為4/5(2至5範圍,更高的分數表明更好的質量)。四個試驗參與者的數量沒有提供信息撤銷或撤回的原因。34- - - - - -3717(74%)的23個試驗樣本容量小於100,其中11例(48%)有少於五十人參加。大麻素暴露持續時間的中位數為2周(範圍8小時至12個月)。參與者暴露於大麻素療法的總數是1932人,445人年大麻素暴露。在1209人分配到對照組(安慰劑或標準治療),有239人每年的接觸;其中,有1121人(占236人年)接受安慰劑。(參與治療的總數和對照組大於樣本大小的總和表1因為參與者在交叉試驗了兩組總數)。
除了一個試驗涉及12個健康cannabis-naive誌願者,48所有參與試驗的患者的病症,如癌症或多發性硬化症、和使用大麻是為了解決化療引起的惡心和嘔吐等症狀或痛苦(見表1)。口服Δ-9-tetrahydrocannabinol或Δ-9-tetrahydrocannabinol-cannabidiol試驗(15)和oromucosalΔ-9-tetrahydrocannabinol-cannabidiol(8試驗)是大麻素製劑的研究。沒有隨機對照試驗的醫療大麻由吸煙被包括在審查,因為不良事件在任何此類研究沒有量化。
不良事件
通過我們的審核,我們發現164人嚴重不良事件分配給大麻素療法和60之間的控製。沒有證據表明嚴重不良事件的發生率更高的醫療大麻使用與控製(率比(RR) 1.04, 95%可信區間0.78 - -1.39)。嚴重不良事件進行分類表2。呼吸道(16.5%)、胃腸道(16.5%)和神經係統疾病(15.2%)是最常報道類別的嚴重不良事件在那些分配給大麻類,而神經係統疾病(30.0%)是最常報道中控製。複發的多發性硬化症(21事件[12.8%]),嘔吐(16個事件[9.8%])和尿路感染(15事件[9.1%])是最常見的嚴重不良事件報道人們之間分配給接收大麻類。大多數的嚴重不良事件(163中用戶和58大麻素控製)是在2試驗報告,貢獻了88.8%的大麻素暴露人年和84.1%的曝光控製。10,11,44
每100人每年15例死亡(3.4)被報道在大麻素用戶(3因為肺炎,1因為子宮頸癌,1因為痙攣,10未指定),和3例死亡(1.3每100人每年)據報道在控製(1)肺炎,1心肌缺血,1未指定)。死亡率這兩組之間的差異沒有統計學意義(相對危險度2.66,95%可信區間0.77 - -9.28)。死亡率RR主要是受到一個隨機對照試驗研究Δ-9-tetrahydrocannabinol對癌因性惡病質症狀的影響(相對危險度2.61,95%可信區間0.33 - -20.37)。44
在23個隨機對照試驗,有4615人不嚴重不良事件分配給大麻素療法(發病率10.37事件/ person-year)和1641事件控製(發病率6.87事件/ person-year)。神經係統疾病是最常見的類別對兩組人群中(占36.7%的事件分配給大麻類和31.3%的事件控製)(表3)。頭暈是最常報道的不嚴重不良事件cannabinoid-exposed參與者;其他不嚴重不良事件的細節如附件2所示(可用www.cmaj.ca / cgi /內容/全/ 178/13/1669 / DC2)。
不嚴重不良事件的發生率明顯高於中對象分配給大麻素療法比控製(相對危險度1.86,95%可信區間1.57 - -2.21)(圖2)。7- - - - - -12,34- - - - - -51研究中我們發現高度的方差(χ的異質性2= 187.42,p< 0.001;我2= 86.7%)。亞組分析類型的大麻素製備降低異質性(附錄3;可以在www.cmaj.ca / cgi /內容/全/ 178/13/1669 / DC2)。不嚴重不良事件的平均率明顯高於人接收oromucosalΔ-9-tetrahydrocannabinol-cannabidiol(相對危險度1.88,95%可信區間1.48 - -2.39)或口頭Δ-9-tetrahydrocannabinol(相對危險度2.18,95%可信區間1.59 - -2.99)比在控製;沒有區別口服Δ-9-tetrahydrocannabinol-cannabidiol和對照組(相對危險度1.31,95%可信區間0.88 - -1.96)。一項研究有不同的曝光時間的幹預(口服Δ-9-tetrahydrocannabinol-cannabidiol 2周)和安慰劑(1周)組和幹預組的發生率明顯降低。51排除本研究增加了口腔的彙集RRΔ-9-tetrahydrocannabinol-cannabidiol從1.31 (95% CI 0.88 - -1.96), 1.54 (95% CI 1.14 - -2.08)。進一步的亞組分析研究設計和研究人口並沒有顯著改變彙集RR為每個醫療大麻素製備不嚴重不良事件(附錄3;可以在www.cmaj.ca / cgi /內容/全/ 178/13/1669 / DC2)。
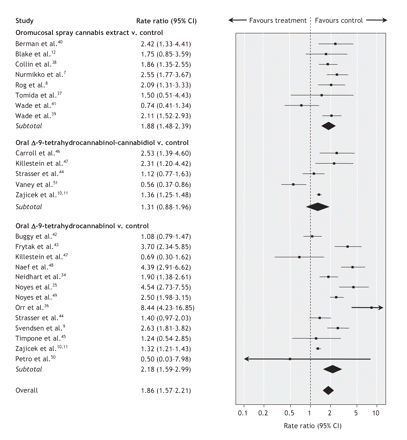
圖2:發病率和速度比率(隨機模型)對不嚴重不良事件參與者分配給醫療大麻素治療或控製在23個隨機對照試驗。垂直虛線代表沒有區別的幹預和控製。CI =置信區間。
8觀察性研究中關注安全問題相關的醫療大麻素製劑,52- - - - - -59總共39嚴重不良事件和3553不嚴重不良事件報告(表4;,可以在附錄4www.cmaj.ca / cgi /內容/全/ 178/13/1669 / DC2)。這些研究有一個對照組。神經係統疾病是最常報道類別對嚴重不良事件(9[23.1%]),不嚴重不良事件(1412 [39.7%])。精神疾病是第二常見的類別(4嚴重不良事件(10.3%)和1265年不嚴重不良事件[35.6%])。報告的不良事件在附錄2(可觀察性研究進行了總結www.cmaj.ca / cgi /內容/全/ 178/13/1669 / DC2)。
解釋
在我們的審查,我們發現8371不良事件相關的醫療大麻素使用,其中4779是在23個隨機對照試驗報告和3592年8觀察性研究。大多數的事件並不嚴重。所有的不良事件報道是意想不到的,根據國際會議協調標準。30.
雖然隨機對照試驗是一種強大的研究設計,不良事件的報告質量的幾個方麵發表試驗中有限的結果。首先,並不是所有的大麻素試驗提供安全信息發布;我們排除了28個隨機對照試驗,包括2試驗研究大麻煙熏的艾滋病毒感染的患者,14,15因為他們沒有量化的不良事件或事件報道隻有一個幹預組。Jadad評分不充分反映安全報告在隨機對照試驗的質量,這意味著評級Jadad量表顯示這些研究方法學質量好,盡管他們可憐的安全報告。第二,大部分的試驗選擇不提供不良事件的絕對數量和參與者報告至少1事件的數量,統一標準推薦的試驗報告(配偶)聲明。60這意味著我們可以隻關注不良事件的發生率,而不是能夠分析事件的發病率和參與者的風險報告至少1事件。第三,由於缺乏數據的頻率為每個患者不良事件,我們必須假設發生的不良事件是獨立的,這不會是一個有效的假設,如果一個病人經曆了超過1事件(可能的情況,不嚴重不良事件)。這種假設會導致代人為縮小CIs在RR估計,這可能影響了測試結果的意義。
我們發現3592不良事件報告8觀察性研究。然而,這些研究都限於缺乏對照組和缺乏調整潛在的混雜因素,如使用煙草、酒精或其他軟性毒品和drug-cannabis交互。
在我們的分析中,我們從研究不包括數據合成大麻素nabilone,因為這個代理有不同的藥代動力學和藥效學特性,及其安全性與Δ-9-tetrahydrocannabinol可能有所不同。盡管nabilone目前用於醫療目的,我們警告說,不能擴展到這種藥物安全數據,和安全的nabilone必須單獨研究。此外,我們排除了吸食大麻的2發表的隨機對照試驗,因為缺乏可量化的不良事件數據。14,15鑒於法律使用醫用大麻的程度和潛在風險管理由吸煙,高質量的安全性和有效性數據抽大麻的迫切需要。我們也警告假設休閑吸食大麻可以預期的副作用發生的醫療大麻素使用。存在的大量使用,並發症和藥物輸送的方法2的數量是不同的,這應該是單獨評估。
我們發現不嚴重不良事件率是1.86倍之間的醫療大麻素比在控製用戶。然而,我們沒有發現更高的嚴重不良事件發生率與醫療有關大麻素使用。嚴重不良事件的99%這一事實隨機對照試驗是在隻有2試驗報告表明,與長期暴露於更多的研究需要進一步描述安全問題。這樣的研究是至關重要的,以發現罕見的不良事件和解決具體問題關於寬容的發展和認知和行為發展的醫療大麻素使用的影響。係統回顧的結果可能刺激未來高質量控製的觀察性研究和臨床試驗探索醫療大麻素使用的安全。我們相信相關係統的數據收集與大麻應該繼續使用,相關的不良事件和結果應公開,協助臨床、監管和政治決策。
@看到相關文章頁麵1685年
腳注
法國ce一個版本的簡曆是能用的一本www.cmaj.ca / cgi /內容/全/ 178/13/1669 / DC1
這篇文章已經被同行評議。
參與者:所有作者的構思和設計研究,負責分析和解釋數據。Tongtong王負責獲取數據。Tongtong小王和馬克製品有完全訪問所有的數據在這項研究中,並最終負責決定提交出版。所有的作者合作起草和修改手稿的重要知識內容,和所有批準出版的最終版本。
確認:我們感謝艾華劉,MSc,流行病學和生物統計學,麥吉爾大學,因為她協助得分的質量研究。
這項研究是由加拿大衛生研究院的研究(批準號MOL66262)。馬克製品是由臨床科學家獎從昏聵de la矯揉造作的魁北克en桑特和露易絲和艾倫·愛德華茲的基礎。
利益衝突:馬克製品已收到基金贈款和谘詢的形式和議長費從製藥公司參與開發和銷售大麻素藥物,包括阿斯利康,拜耳,Cannasat,瓦製藥、蘇威和Valeant;然而,他沒有經濟利益,也不是他的員工,這些公司。沒有利益衝突聲明Tongtong Wang jean - paul夾頭或斯坦·夏皮羅。










